O processo é o mesmo para todos os tipos de
baterias de chumbo-ácido
Baterias inundadas, em gel e AGM. As ações que ocorrem durante a descarga são o inverso daquelas que ocorrem durante a carga.
O material descarregado em ambas as placas é sulfato de chumbo (PbSO4). Quando uma tensão de carga é aplicada, ocorre o fluxo de carga. Os elétrons se movem nas partes metálicas; íons e moléculas de água se movem no eletrólito.
Ocorrem reações químicas tanto nas placas positivas quanto nas negativas, convertendo o material descarregado em material carregado. O material nas placas positivas é convertido em dióxido de chumbo (PbO2); o material nas placas negativas é convertido em chumbo (Pb).
O ácido sulfúrico é produzido em ambas as placas e a água é consumida na placa positiva.
Se a voltagem for muito alta, outras reações também ocorrerão. O oxigênio é arrancado das moléculas de água nas placas positivas e liberado como gás. O gás hidrogênio é liberado nas placas negativas — a menos que o gás oxigênio consiga chegar às placas negativas primeiro e se recombine em H₂O. Uma bateria liberará gases perto do final da carga porque a taxa de carga é muito alta para a bateria suportar. Um carregador com compensação de temperatura e regulação de voltagem, que reduz automaticamente a taxa de carga à medida que a bateria se aproxima do estado totalmente carregado, elimina a maior parte dessa liberação de gases. É extremamente importante não carregar baterias por longos períodos em taxas que causem a liberação de gases, pois elas utilizam água, que em baterias seladas com válvulas reguladas não pode ser reposta. Obviamente, nenhuma bateria deve ser sobrecarregada por um longo período... mesmo em baixas taxas usando as chamadas "cargas de manutenção".
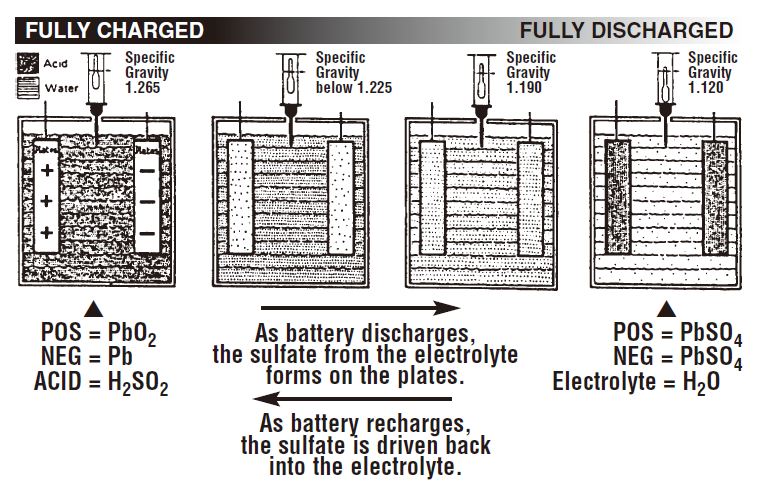
Em uma bateria totalmente carregada, a maior parte do sulfato está no ácido sulfúrico. À medida que a bateria descarrega, parte do sulfato começa a se formar nas placas como sulfato de chumbo (PbSO4). Conforme isso acontece, o ácido fica mais diluído e sua densidade diminui, pois a água substitui uma quantidade maior de ácido sulfúrico. Uma bateria totalmente descarregada tem mais sulfatos nas placas do que no eletrólito.
A ilustração a seguir mostra a relação entre as leituras de densidade específica e a combinação do sulfato do ácido com as placas positiva e negativa em vários estados de carga.
Quão crítica é a tensão de recarga? Por que todas as baterias VRLA são tão sensíveis à carga?
Todas as baterias de chumbo-ácido liberam hidrogênio da placa negativa e oxigênio da placa positiva durante o carregamento.
Baterias VRLA
Possuem válvulas sensíveis à pressão. Sem a capacidade de reter a pressão dentro das células, o hidrogênio e o oxigênio seriam perdidos para a atmosfera, eventualmente secando o eletrólito e os separadores.
Voltagem é a pressão elétrica. Carga (ampères-hora) é a quantidade de eletricidade armazenada. Corrente (ampères) é o fluxo elétrico (velocidade de carregamento). Uma bateria só pode armazenar uma certa quantidade de eletricidade. Quanto mais próxima da carga completa, mais lenta deve ser a recarga.
A temperatura também afeta o carregamento. Se a pressão (voltagem) correta for usada para a temperatura, a bateria aceitará carga na sua taxa ideal. Se for usada pressão excessiva, a carga será forçada através da bateria mais rapidamente do que pode ser armazenada. Reações diferentes da reação de carregamento ocorrem para transportar essa corrente através da bateria — principalmente a gaseificação.
O hidrogênio e o oxigênio são liberados mais rapidamente do que a reação de recombinação. Isso aumenta a pressão até que a válvula de alívio de pressão se abra. O gás perdido não pode ser reposto. Qualquer bateria VRLA irá secar e falhar prematuramente se sofrer sobrecarga excessiva.
Nota: É a pressão (voltagem) que inicia esse problema — uma bateria pode ser "sobrecarregada" (danificada por excesso de voltagem) mesmo que não esteja totalmente "carregada".
Por isso, a tensão de carregamento deve ser cuidadosamente regulada e a temperatura compensada para os valores adequados.

